2025年第三季度審評中心保健食品審評審批動態
2025-11-03
2025年第三季度,國家市場監督管理總局食品審評中心(以下簡稱“審評中心”)穩步推進保健食品審評審批各項工作,從審評意見出具到核查確認、批件發放等全流程高效銜接,為保健食品行業規范發展提供了有力保障。本動態基于審評中心公開的官方數據,從政策發布、審評意見發放、核查與批件發放等維度展開詳細分析。
PART1 政策發布
第三季度,審評中心圍繞行業實操痛點與合規需求,密集發布3項關鍵政策文件,為企業辦理相關業務提供明確指引。
《“雙無” 保健食品換證常見問題及解答(第三批)》《“雙無” 保健食品換證常見問題及解答(第四批)》:持續回應企業在 “雙無” 保健食品換證過程中的高頻疑問,進一步細化操作流程,降低企業合規成本。
《保健食品注冊證書部分注冊人注銷變為單方持有技術轉讓辦理指引》:針對注冊人注銷后證書單方持有場景下的技術轉讓業務,明確辦理標準與流程,規范行業資源整合中的審批銜接。
PART2 審評意見通知書發放
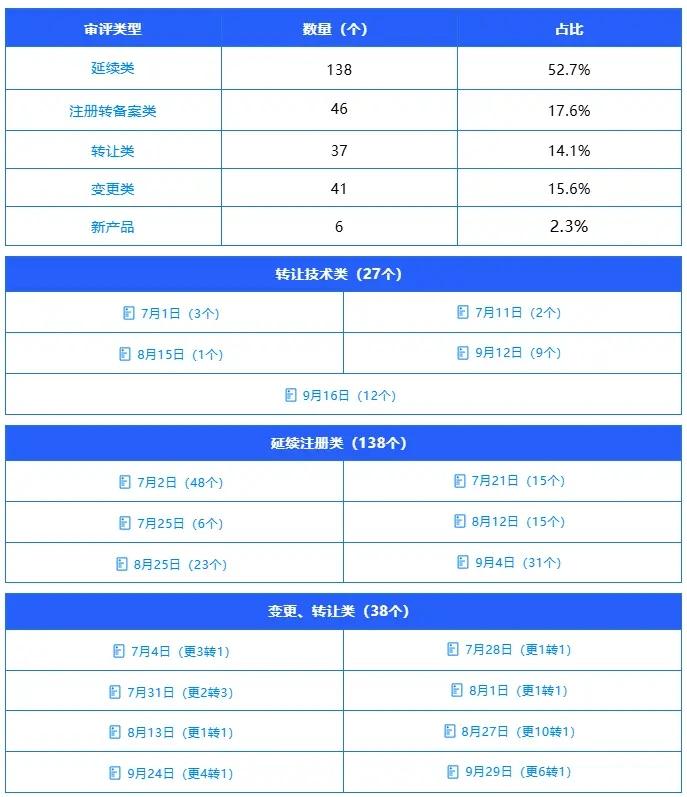
2025年第三季度國家市場監督管理總局食品審評中心共發布審評意見通知書262個,覆蓋轉讓、延續、變更、注冊轉備案及新產品五大核心類別,具體數據及分析如下:
延續類:138個(占比52.7%),反映行業存量產品合規延續需求集中,也體現出審評中心對成熟產品合規性審核的高效把控。
注冊轉備案類:46個(占比17.6%),自保健食品注冊與備案雙軌制實施以來,注冊轉備案通道持續暢通,本季度的審批數據表明,符合備案條件的原注冊產品正有序完成類別轉換,行業產品管理體系進一步優化。
轉讓類:37個(占比14.1%),轉讓類審批活躍體現出保健食品行業資源整合步伐加快,部分企業通過產品轉讓實現資源優化配置。
變更類:41個(占比15.6%),變更類審批則主要集中在技術要求等方面,反映出企業根據市場需求和監管要求及時升級和規范產品的合規意識增強。
新產品:數量保持低位,凸顯注冊申報的科學性門檻,也反映出行業在新原料應用、功能聲稱創新等方面仍存在提升空間,未來需進一步激發企業研發創新活力。
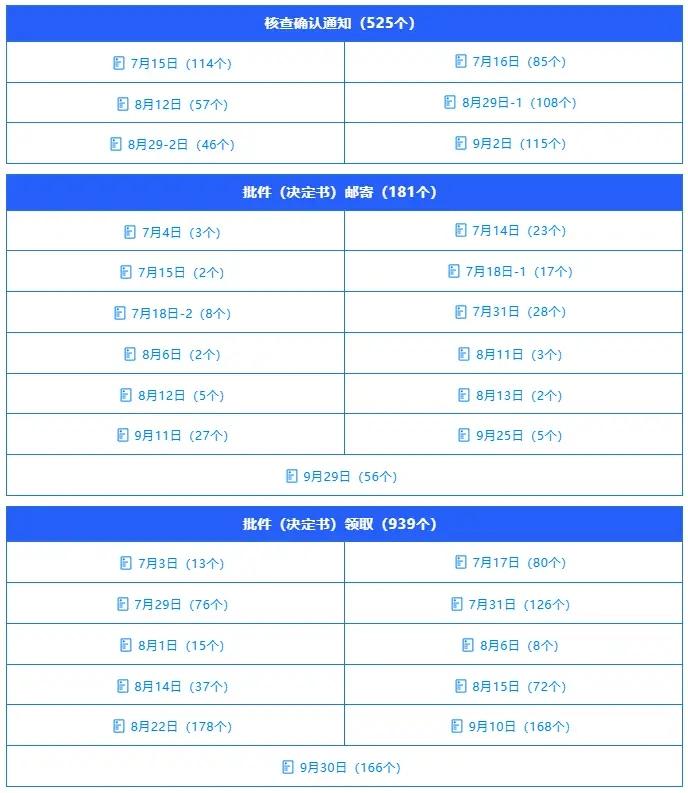
PART3 核查通知與批件發放
在審評意見出具的基礎上,審評中心同步推進核查確認與批件發放等后續環節,保障審批流程閉環管理,各項工作指標均保持較高效率:本季度共郵寄核查確認通知 525 個,核查工作規模顯著高于審評意見發放數量,凸顯核查是本季度審評工作的核心重點,也體現出審評中心對產品真實性、合規性的核查力度持續加強;同時完成批件(決定書)郵寄 162 個、通知領取 939 個,兩類批件流轉渠道合計覆蓋 1101 個審批事項。